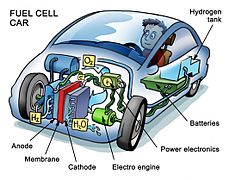
Pile à combustible
Dans cette partie, nous allons voir comment exploiter l'hydrogène que l'on extrait. C'est grâce à cet hydrogène que l'on peut construire une pile à combustible.
I. Le fonctionnement de la pile à combustible
Tout d'abord, le principe de la pile à combustible est de convertir l'énergie chimique en énergie électrique. La pile est constituée d'une anode et d'une cathode, l'hydrogène que l'on a extrait alimentera l'anode et l'oxygène (qui se trouve dans l'air) alimentera la cathode, ces molécules vont permettre le fonctionnement de la pile via des réactions.
Au niveau de l'anode une réaction d'oxydation aura lieu, on la voit dans l'image ci-dessous.
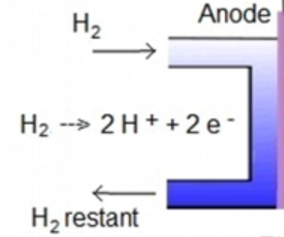
Au niveau de la cathode, il y aura une réaction de réduction.
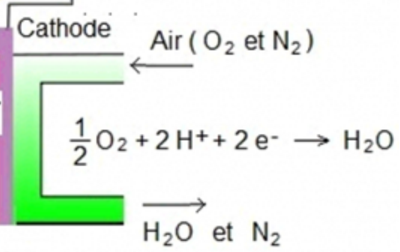
L'anode et la cathode sont séparées par 2 couches fines de platine (qui jouent le rôle de catalyseur)et ces 2 couches sont séparées par une membrane échangeuse de proton. Cette membrane ne laisse passer que les protons et non pas les électrons. Pour que les électrons circulent, il faut placer un circuit extérieur reliant l'anode et la cathode. On peut voire ci-dessous le schéma complet d'une pile à hydrogène.
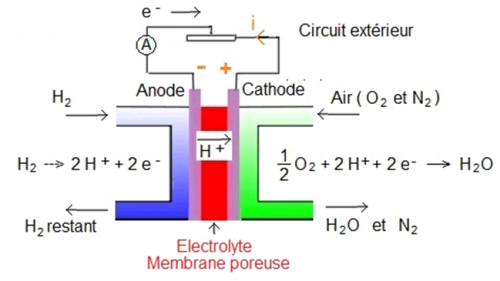
La pile rejette du diazote (N2), de l'eau (H2O) et le dihydrogène restant (H2).
II. L'efficacité de la pile à hydrogène
L'importance d'extraire de l'hydrogène se base sur les différentes machines que l'on peut créer avec l'hydrogène. Pour vérifier que la construction de ces machines nous apporte un bon rendement, il faut assurer une éfficacité énergétique élevée. Grâce à la formule :
η : Efficacité énergetique de la pile
ΔG : Variation d'enthalpie libre (Joule/Mol)
ΔH : Variation d'enthalpie (Joule/Mol)
on calcule de manière théorique l'efficacité énergetique et on trouve 83%. On en déduit que l'efficacité de la pile est élevée. Grâce à cette pile, la création de nouvelles machines peut être exploitable comme par exemple la voiture à hydrogène.